FGF23関連低リン血症性くる病・骨軟化症
FGF23とは
FGF23は2000年にFGFファミリー最後のメンバーとして同定された内分泌因子です。FGF23は骨の中に存在する成熟骨細胞で産生されたのちに血中に分泌され、腎臓において腎近位尿細管でのリンの再吸収抑制と、1α水酸化酵素発現抑制を介した活性型ビタミンD: 1,25(OH)2Dの発現低下という2つの経路を介して血中リン濃度を低下させます(図1)。その後の研究で、FGF23ノックアウトマウスでは高リン血症や高1,25(OH)2D血症を認めることなどから、FGF23が血清リン濃度の主たる生理的調整因子ということが分かっています。

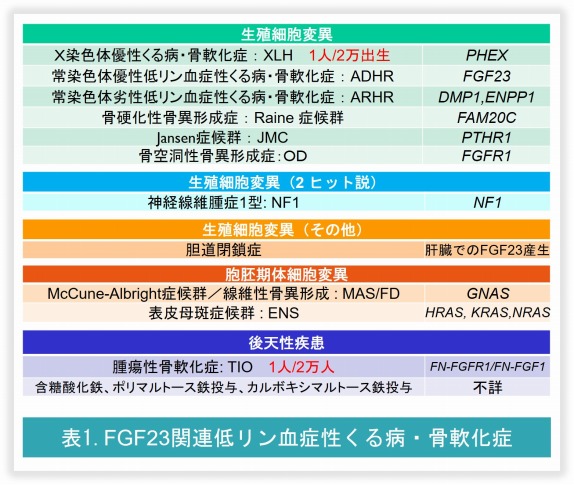
FGF23が主要な血中リン濃度調節因子であると同定された後に、それまで原因が明らかでなかったリン代謝異常症(低リン血症性くる病・骨軟化症、高リン血症性腫瘍状石灰沈着症)の一部がFGF23の作用過剰や減弱により惹起されることが明らかとなりました(表1)。
更には、慢性腎不全の進行に伴いリン排泄障害が進行するのと同時にFGF23が代償性に血中濃度を増加させており、実際の血中リン濃度の上昇を伴わない慢性腎不全の比較的早期からFGF23が高値となっていることや、それによって1,25(OH)2Dが低下し、その後徐々に進行する高リン血症と相まって続発性副甲状腺機能亢進症を惹起するなどといった、これまでの副甲状腺ホルモン(PTH)と1,25(OH)2Dのみでは説明が困難であった慢性腎不全の進行に伴うカルシウム・リン代謝異常(CKD-MBD)の進展に関する詳細なメカニズムが明らかとなりました。
FGF23の基礎研究
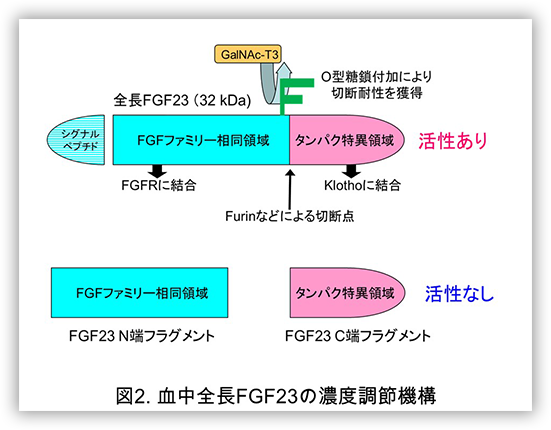
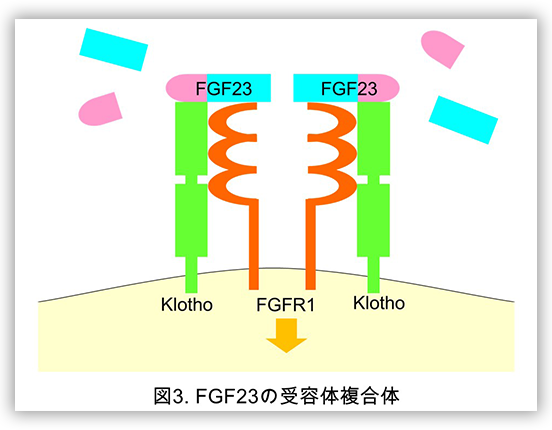
また基礎研究においてはFGF23がFurinなどの酵素によって切断されることで、その生体内での活性が調整されており、その酵素切断からの保護にはたらくGalNac-T3の働きが実際の活性型FGF23の血中濃度調整に重要である事や(図2)、FGF23の腎尿細管での受容体は従来老化に関与すると考えられてきたKlothoとFGFR1の複合体であることなどが明らかとなっています(図3)。
一方で、骨細胞がどのようにして血中のリン濃度を感知してFGF23の産生を調節しているかは近年まで明らかでなかったのですが、2019年に当研究室と徳島大学 藤井節郎記念医科学センターとの共同研究によりFGFR1がリン感知機構の中心となる分子であることを明らかにしています。今後も更に生体のリン感知機構の解明を中心とした研究を進めていく予定です。
誤診されやすい骨軟化症
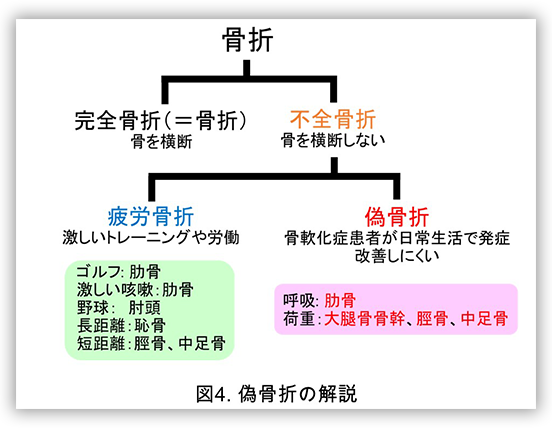
臨床の現場では、FGF23産生腫瘍により主に成人で発症する腫瘍性骨軟化症(Tumor induced osteomalacia: TIO)が、他の骨軟化症と同様に全身の偽骨折(図4)による骨痛や筋痛、筋力低下などを呈して整形外科や膠原病・リウマチ内科、神経内科などを受診するものの脊柱管狭窄症や慢性関節リウマチ、線維筋痛症などと誤診され、適切な治療を受けることが出来ないでいる患者さんが非常に多いという状況です(表2)。中には寝たきりとなるような患者さんもおられるため、本症を含める骨軟化症を惹起する疾患を総じての他科への啓発活動が急務かと思われます。当研究室では整形外科や膠原病・リウマチ内科で外来を担当する先生方を対象として、続発性骨粗鬆症の原因として比較的頻度の高い原発性副甲状腺機能亢進症と、骨粗鬆症類縁疾患の原因として比較的頻度の高い骨軟化症を外来で簡便にスクリーニングするための①カルシウム、②リン、③アルカリホスファターゼ、④アルブミンの採血を推奨しています(表3)。


FGF23関連低リン血症性くる病・骨軟化症の臨床診断
またこれまでは低リン血症性骨軟化症の診断に至っても、原因となる疾患の正確な診断に至らなかった例も多いと考えらます。しかしFGF23の同定後にはFGF23の測定系が開発され、FGF23作用過剰による低リン血症性疾患では、血中FGF23濃度が30 pg/ml以上を、それ以外のビタミンD欠乏症/依存症やファンコーニ症候群などでは血中FGF23濃度が30 pg/ml未満を示すことがガイドライン上に明記されています(図5)。

FGF23測定
FGF23の測定は2019年12月に保険適用となりました。ただし対象は低リン血症性くる病・骨軟化症のみとなりますのでご注意ください。また測定回数は基本的にFGF23関連低リン血症性くる病・骨軟化症を診断する際の1回のみとなります。ただし、腫瘍性骨軟化症の術後や、一部の鉄剤によるFGF23関連低リン血症性くる病・骨軟化症での薬剤中止後は改善を確認するための測定が1度限りで可能です。また既に下記抗FGF23抗体(ブロスマブ:クリースビータ®)を治療に使用している場合は異常値がでるために保険診療上での測定はできませんので併せてご注意ください。
測定依頼法
1 測定を希望する旨と検体数を、依頼書を添付のうえ下記までメールで御一報下さい。
左の依頼書は、電子メールに添付して御送付下さい。

(簡単な病歴を記載する空白蘭を追加、採血項目にALP、骨型ALP、TRACP-5bを追加してください)
依頼書は、灰色の色が付いた部分に御記入下さい。
検査結果は、すべての項目を記入戴かなくても結構です。
記入例が2枚目のシートに付いています。その他の情報は、コメント欄に御記入下さい。
加藤 創生 katoha-int@h.u-tokyo.ac.jp
古家 美菜絵 koga-tky@umin.ac.jp
2 当方からの返事を御確認後、検体(冷凍血清約1 ml、血漿でも可)を平日午前着で御送付下さい。
結果は、通常1ヶ月以内に通知いたします。
至急の場合は、お知らせ下さい。
費用は当方で負担いたします。
検体送付先
〒113-8655 文京区本郷7-3-1
東京大学医学部附属病院 腎臓・内分泌内科 加藤 創生、古家 美菜絵
注意点
FGF23の測定に当たっては、各施設での倫理委員会の承認、患者様からの同 意取得等、倫理面に御配慮下さい。御希望の場合には、当院で使用している説明書、同意書をお送りいたします。
注意点
個人情報保護の観点から、当方では患者様を同定できる情報は必要ありま せん。但し、年齢によりリンの基準値が異なること、伴性遺伝性疾患を対 象疾患に含むことから、年齢と性別はお知らせ下さい。
FGF23関連低リン血症性くる病・骨軟化症の種類、症状
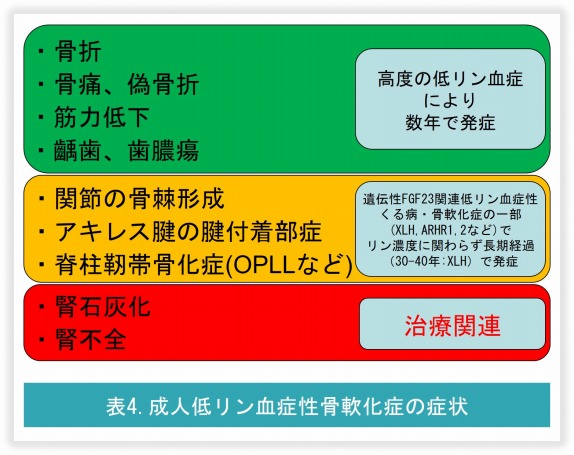
現在FGF23の不適切な産生が原因となりFGF23関連低リン血症性くる病・骨軟化症を呈する疾患には表1のものが知られています。遺伝性のFGF23関連低リン血症性くる病のなかのX染色体伴性低リン血症性くる病(XLH)は、出生率がおよそ2万人に1人であり、先天性の低リン血症性くる病の原因疾患として最多となります。しかしながらあまりこれまでに大規模な臨床研究がXLHに対してなされていなかったこともあり、合併症である偽骨折(図4)や骨折、また成人XLH症例に認める長期の合併症と思われる変形性関節症、後縦靭帯骨化症/黄色靭帯骨化症(表4)などの発症率と、治療によるこれらの合併症の予防効果に関しては未だ明らかでないところがあります。このようなXLHの臨床像をより明らかにするべく、現在XLHの大規模な長期観察研究を日韓の多施設で2018年より開始しています。当施設では特に成人XLHを1名でも多く登録したいと考えておりますので、患者さんをご紹介頂ければ幸いです。
FGF23関連低リン血症性くる病・骨軟化症の遺伝子診断
また表1の遺伝性FGF23関連低リン血症性くる病に関しては、XLH (PHEX)、ADHR (FGF23)、ARHR1 (DMP1)、ARHR2 (ENPP1)、Raine症候群 (FAM20C)、Jansen症候群 (PTHR1)、Osteoglophonic dysplasia (FGFR1)の全エクソン領域を同時に解析できる遺伝子診断パネルを用意しています(表5)。FGF23関連低リン血症性骨軟化症と診断されている患者さんで、遺伝子診断までご希望の方がおられましたらぜひご受診/ご紹介を御検討ください。

腫瘍性骨軟化症の原因腫瘍同定におけるオクトレオスキャン®と全身静脈FGF23サンプリング
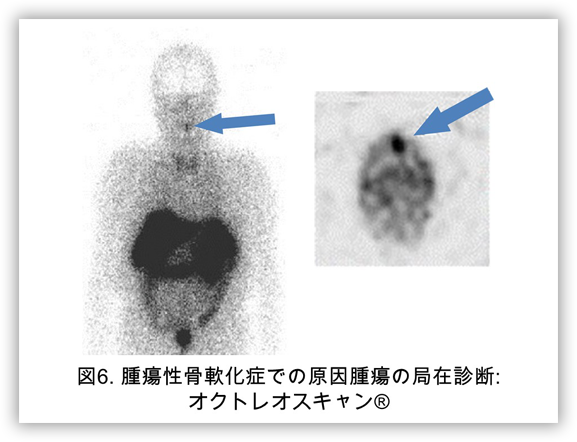
一方で腫瘍性骨軟化症では原因腫瘍(FGF23産生腫瘍)の局在診断が出来れば、腫瘍の拡大切除を行うことでの根治治療が可能ですが(腫瘍の残存があると、FGF23産生腫瘍の構成細胞に血中リン濃度感知閾値の低下が生じていることから、残存腫瘍からのFGF23産生が亢進するため低リン血症の改善を望めません)、腫瘍が全身の骨や軟部組織に発生しうることや、サイズが小さいことも多く局在診断が困難である症例にしばしば遭遇します。また画像でみつかった腫瘍のFGF23産生能も腫瘍切除前に確認しなくてはなりせん。当研究室ではFGF23産生腫瘍の機能的な局在診断のための、オクトレオスキャン®と全身静脈でのFGF23サンプリングの組み合わせでの実施の有効性の評価を特定臨床研究として行っております。
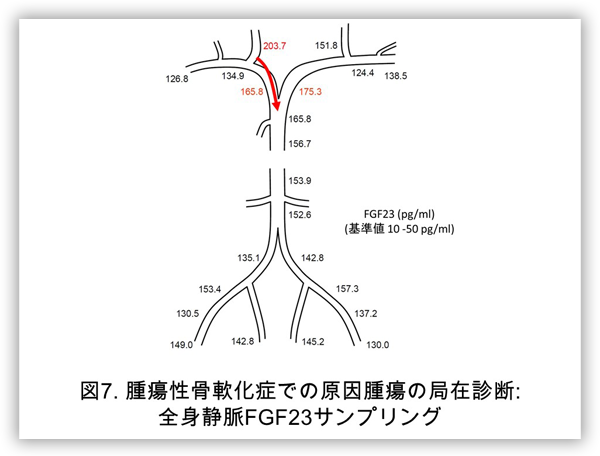
具体的には①最初にオクトレオスキャン®とFDG-PETを施行しFGF23産生腫瘍として疑わしい腫瘍が内科を確認します。しかしオクトレオスキャン®で取り込みがあっても、様々なタイプの腫瘍や炎症部位に取り込まれことが分かっており、FDG-PETよりはよりホルモン産生腫瘍に取り込まれやすい傾向があるといった程度です。そこで、次いで②全身静脈の22か所にFDG-PETやオクトレオスキャン®で取り込みを認めた部位の周辺での採血部位を増やしたサンプリングポイントを用いて、静脈カテーテルを利用して全身のFGF23サンプリングを施行します。①で取り込みを認めた部位の近位部でのFGF23の上昇を確認することで腫瘍のFGF23産生能を確認し、拡大切除術に進みます。
実際にFDG-PETやオクトレオスキャン®で取り込みを認めたものの、近位部のFGF23の上昇を認めず、他の部位でFGF23産生腫瘍を新たに同定した症例や、FDG-PETやオクトレオスキャン®のみでは腫瘍病変を検出できなかったものの、全身静脈FGF23サンプリングの結果からFGF23産生腫瘍を同定できた症例などもあり、これらの機能的検査は相補的であるため、FGF23産生腫瘍の局在診断時には全例で施行すべき検査と考えております。
当院では他の病院で原因となるFGF23産生腫瘍が同定できなかった腫瘍性骨軟化症疑い症例が多く紹介されてきますが、2019年4月時点で腫瘍性骨軟化症疑い症例42例中34例(80%)で腫瘍の局在診断に至っております。現在も実施症例数を増やして将来の全身静脈FGF23サンプリングの保険適用を目指しておりますので、腫瘍性骨軟化症が疑われる患者さんがおられましたらご紹介頂けますと幸いです。
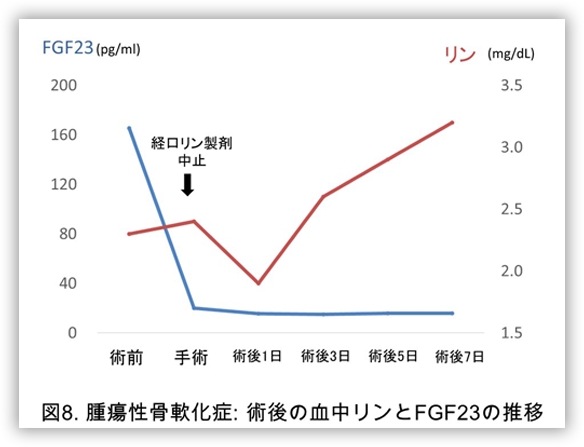
添付する腫瘍性骨軟化症の症例は58歳男性の方で、14年前から全身の疼痛と歩行障害が出現し車椅子移動となり強直性脊椎炎と診断されていました。9年前にFGF23が120 pg/ml (> 30)と高値であることから腫瘍性骨軟化症疑いとされましたが、CT、MRIでは腫瘍の局在診断に至らず、従来の活性型ビタミンDと経口リン製剤で加療するものの骨痛と筋力低下により松葉杖2本での移動までの改善にとどまっていました。当科にてオクトレオスキャンと全身静脈サンプリングを施行し上歯槽骨内のFGF23産生腫瘍を同定し拡大切除したことで低リン血症が改善し職場復帰を果たしています(図6,7,8)。
FGF23関連低リン血症性くる病・骨軟化症の現行治療での問題と新規治療法
腫瘍が同定できない、または拡大切除ができない腫瘍性骨軟化症症例や、X染色体伴性低リン血症性くる病といったFGF23関連低リン血症性くる病・骨軟化症の治療においては、活性型ビタミンDと経口リン製剤が使用されています。しかしいずれのFGF23関連低リン血症においても血中リン濃度感知閾値の低下が原因で起きているため、実際に血中リン濃度を正常化させることは難しく、また血中リン濃度の正常化を目指して大量の経口薬を投与すると、尿中カルシウム排泄の著増による腎性尿崩症が生じ、脱水による腎前性腎不全とそれを繰り返す事での慢性腎不全への進展リスクが高まります。従ってFGF23関連低リン血症性くる病・骨軟化症での慢性腎不全進展のリスク回避を考慮した血中リン濃度の治療目標は経口リン製剤内服前で正常下限以下、経口リン製剤内服後1-2時間で正常低値となります。しかしこれでは骨石灰化の完全な正常化は望めず、やはり易骨折性や骨軟化症の慢性期の合併症である変形性関節症や後縦靭帯骨化症/黄色靭帯骨化症などの発症を予防することができません(表4)。この従来治療法のアンメットニーズに対して、より病態に則した治療として開発されたのが抗FGF23抗体: ブロスマブ(クリースビータ®)で、2018年以降、欧州、北米でXLHやTIO症例に対して保険適用となっています。本邦でも2019年12月よりXLH、TIOを含めたFGF23関連低リン血症性くる病・骨軟化症に対して広く保険適用となりました。上記FGF23の測定も保険適用となっておりますので、適切にFGF23関連低リン血症性くる病・骨軟化症の診断をおこない「ビタミンD抵抗性くる病・骨軟化症(くる病・骨軟化症)」としての難病申請を行い受理された上で、本治療が必要と考えられるご症例での使用を御検討ください。
関連リンク

FGF23関連低リン血症性くる病・骨軟化症-低リン血症とは?

FGF23関連低リン血症性くる病・骨軟化症とはどんな病気?

FGF23関連低リン血症性くる病・骨軟化症-症状、検査、診断

FGF23関連低リン血症性くる病・骨軟化症-治療

FGF23関連低リン血症性くる病・骨軟化症 疾患情報サイト
「くるこつ広場」
